2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test
-
Aşağıdaki seçeneklerin hangisinde kimyasal türün örneği yanlış verilmiştir?
A) Atom Ca
B) Bileşik H2
C) Molekül CO2
D) İyon CO32-
E) Molekül CO
-
Periyodik sistemde aynı periyottaki soygazlara yaklaştıkça aşağıdakilerden hangisi azalır?
A) Değerlik elektron sayısı
B) Elektron sayısı
C) Metalik Özellik
D) İyonlaşma Enerjisi
E) Atom numarası
-
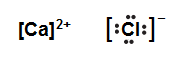
Kararlı iyonlarının Lewis yapıları yukarıdaki gibi olan Ca ve Cl atomlarının oluşturacağı bileşiğin formülü ve bağ türü aşağıdakilerden hangisinde doğru verilmiştir?A) Ca+2Cl-1 İyonik
B) Ca2Cl Kovalent
C) CaCl2 Kovalent
D) CaCl2 İyonik
E) Ca2Cl İyonik
-
I. İyonik bağlar
II. Kovalent bağlar
III. Metalik bağlar
IV. Hidrojen bağları
Yukarıda verilen bağ türlerinden hangisi ya da hangileri atomlar arası bağ türüdür?A) Yalnız IV B) I ve II C) I, II ve III
D) I, II ve IV E) I, II, III ve IV
-

Elif, 4, 7N, 10Ne ve 12 Mg atomlarının Lewis yapılarını yukarıdaki gibi yazmıştır.
Buna göre Elif, hangi atomların Lewis yapılarını doğru yazmıştır?A) Be ve N B) N ve Ne
C) Mg ve Be D) Ne ve Mg
E) Be ve N
-
2.periyot 2A grubunda bulunan elementin nötron sayısı, proton sayısından 3 fazladır.
Bu elementin kütle numarası kaçtır?A) 11 B) 12 C) 13 D) 14 E) 15
-
X+ iyonu ile 10Ne atomunun eletron sayısı aynıdır.
Buna göre X atomunun periyodik sistemdeki yeri neresidir?A) 1. Periyot 8A Grubu
B) 2. Periyot 7A Grubu
C) 3. Periyot 1A Grubu
D) 2. Periyot 1A Grubu
E) 3. Periyot 7A Grubu
-
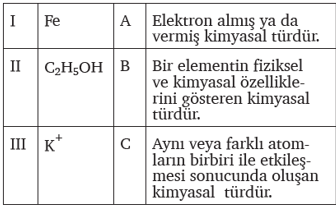
Yukarıda verilen kimyasal tür tanım eşleştirmeleri hangi seçenekte doğru verilmiştir?A) I - B II - A III - C
B) I - A II - C III - B
C) I - C II - B III - A
D) I - B II - C III - A
E) I - C II - A III - B
-
Aşağıda formülleri verilen bileşiklerden hangisinin adı yanlıştır?
A) CO Karbon dioksit
B) P2O3 Difosfor trioksit
C) SO2 Kükürt dioksit
D) N2O5 Diazot pentaoksit
E) CCl4 Karbon tetraklorür
-
11X7Y9Z elementlerinin yaptıkları X3Y, Y2, Y2Z molekillerinin molekül içinetkileşim türü aşağıdakilerden hangisinde sırasıyla doğru olarak verilmiştir?
A) İyonik - Apolar Kovalent - Polar Kovalent
B) İyonik - Polar Kovalent - Apolar Kovalent
C) Polar Kovalent - İyonik - İyonik
D) Polar Kovalet - İyonik - Polar Kovalent
E) Apolar Kovalent - Polar Kovalent - İyonik
-
Aşağıdaki cümleleri okuyarak doğru olan yargıların başına (D), yanlış olana (Y) yazınız
[......] Elementler sembol, bileşikler ise formüllerle gösterirler.
[......] Rutherford, atomun yapısında büyük boşluklar olduğu fikrini ileri sürmüştür.
[......] Paschen ışıması, n=4,5,6... seviyelerinden n=3 seviyesine olan ışımaları ifade eder.
[......] Pauli’ nin Belirsizlik Kuramı’ na göre bir elektronun yeri ve hızı aynı anda tespit edilemez.
[......] Triatlar Kuramı olarak bilinen kural ilk kez Alexander John Newlans tarafından ortaya atılmıştır.
-
Aşağıda verilen cümlelerde verilen boşlukları uygun kavramlarla doldurunuz
a. Modern periyodik tabloda elemetler, artan ……………..numaralarına göre yan yana sıralanmışlardır.
b. ………………… ‘ ya göre dört temel element; “Hava, Toprak, Su ve Ateş” tir.
c. Periyodik tabloda 3. Periyot 5A grubunda bulunan element, …………..sembolü ile gösterilir.
d. Periyodik tablonun 4 ve 5 nci periyotlarında …………’ er tane element bulunmaktadır.
e. 2A grubu elementleri olarak bilinen elementlerin özel adı …………………………….Metalleridir.
-
Aşağıdakilerden hangisi periyodik sistemin oluşuman katkı sunmamıştır?
A) Mendelev B) Moseley C) Franklin
D) Meyer E) Döbereiner
-
Mdern periyodik tablo ile ilgili aşağıdakilerden hangisi yanlıştır?
A) Yatay sıralara periyot denir.
B) Düşey sütunlara grup denir.
C) Eşit sayıda grup ve periyot vardır.
D) Elementler artan atom numaralarına göre sıralanmıştır.
E) Her element için sadece bir tane kutucuk ayrılmıştır.
-
I. Bir atomun elektron sayısı kadar iyonlaşma enerjisi vardır.
II. Kolay kopan elektronlara değerlik elektronları denir.
III. Aynı grupta yukarıdan aşağıya doğru inildikçe iyonlaşma enerjisi azalır.
Yukarıda verilen ifadelerden hangisi veya hangileri doğrudur?A) I, II ve III B) I ve III C) I ve II
D) II ve III E) Yalnız I
-
I. Elementlerin fiziksel ve kimyasal özelliklerinin değişimi atom yarıçapına bağlıdır.
II. Periyodik sistemde aynı grupta yukarıdan aşağıya doğru katma sayısı arttıkça atom yarıçapı artar.
III. Aynı periyotta soldan sağa doğru katman sayısı değişmez.
Yukarıda verilen ifadelerden hangisi veya hangileri doğrudur?A) I, II ve III B) I ve III C) I ve II
D) II ve III E) Yalnız I
-
Aşağıdakilerden hangisi ametal değildir?
A) H B) C C) N D) O E) B
-
Aşağıdakilerden hangisi yarı metaller için doğru değildir?
A) Metallerle ametallerin arasında yer alırlar.
B) Parlak veya mat olabilirler.
C) Gaz halinde bulunurlar.
D) Hem pozitif hem de negatif yüklü iyon haline geçebilirler.
E) Hem metallerin hem de ametallerin özelliklerini taşırlar.
-
I. Periyodik sistemde elementlerin büyük çoğunluğunu oluşturur.
II. Genellikle son katmanlarında 1, 2, 3 elektron bulundururlar.
III. Hidrojen ve bor hariç 1A, 2A 3A grupları, geçiş ve iç geçiş elementleri metaldir.
Metallerle ilgili yukarıda verilenlerden hangisi veya hangileri doğrudur?A) Yalnız I B) I ve II C) II ve III
D) I ve III E) I, II ve III
-
I. Yatay satırlara periyot denir.
II. Düşey sütunlara grup denir.
III. 7 periyot ve 18 gruptan oluşur.
Modern periyodik tablo ile ilgili yukarıda verilenlerden hangisi veya hangileri doğrudur?A) Yalnız I B) I ve II C) II ve III
D) I ve III E) I, II ve III
-
Kütle numaraları aynı, nötron ve atom numaraları farklı olan atomlara ................. atomlar denir.
Yukarıda verilen boşluğa hangisi getirilmelidir?A) izotop B) izoton C) izobar
D) izoelektronik E) izoprotonik
-
Nötron sayıları aynı, proton sayıları faklı olan atomlara ................. atomlar denir.
Yukarıda verilen boşluğa hangisi getirilmelidir?A) izotop B) izoton C) izobar
D) izoelektronik E) izoprotonik
2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test CEVAPLARI
-
Aşağıdaki seçeneklerin hangisinde kimyasal türün örneği yanlış verilmiştir?
A) Atom Ca
B) Bileşik H2
C) Molekül CO2
D) İyon CO32-
E) Molekül CO -
Periyodik sistemde aynı periyottaki soygazlara yaklaştıkça aşağıdakilerden hangisi azalır?
A) Değerlik elektron sayısı
B) Elektron sayısı
C) Metalik Özellik
D) İyonlaşma Enerjisi
E) Atom numarası -
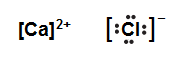
Kararlı iyonlarının Lewis yapıları yukarıdaki gibi olan Ca ve Cl atomlarının oluşturacağı bileşiğin formülü ve bağ türü aşağıdakilerden hangisinde doğru verilmiştir?A) Ca+2Cl-1 İyonik
B) Ca2Cl Kovalent
C) CaCl2 Kovalent
D) CaCl2 İyonik
E) Ca2Cl İyonik -
I. İyonik bağlar
II. Kovalent bağlar
III. Metalik bağlar
IV. Hidrojen bağları
Yukarıda verilen bağ türlerinden hangisi ya da hangileri atomlar arası bağ türüdür?A) Yalnız IV B) I ve II C) I, II ve III
D) I, II ve IV E) I, II, III ve IV -

Elif, 4, 7N, 10Ne ve 12 Mg atomlarının Lewis yapılarını yukarıdaki gibi yazmıştır.
Buna göre Elif, hangi atomların Lewis yapılarını doğru yazmıştır?A) Be ve N B) N ve Ne
C) Mg ve Be D) Ne ve Mg
E) Be ve N -
2.periyot 2A grubunda bulunan elementin nötron sayısı, proton sayısından 3 fazladır.
Bu elementin kütle numarası kaçtır?A) 11 B) 12 C) 13 D) 14 E) 15
-
X+ iyonu ile 10Ne atomunun eletron sayısı aynıdır.
Buna göre X atomunun periyodik sistemdeki yeri neresidir?A) 1. Periyot 8A Grubu
B) 2. Periyot 7A Grubu
C) 3. Periyot 1A Grubu
D) 2. Periyot 1A Grubu
E) 3. Periyot 7A Grubu -

Yukarıda verilen kimyasal tür tanım eşleştirmeleri hangi seçenekte doğru verilmiştir?A) I - B II - A III - C
B) I - A II - C III - B
C) I - C II - B III - A
D) I - B II - C III - A
E) I - C II - A III - B -
Aşağıda formülleri verilen bileşiklerden hangisinin adı yanlıştır?
A) CO Karbon dioksit
B) P2O3 Difosfor trioksit
C) SO2 Kükürt dioksit
D) N2O5 Diazot pentaoksit
E) CCl4 Karbon tetraklorür -
11X7Y9Z elementlerinin yaptıkları X3Y, Y2, Y2Z molekillerinin molekül içinetkileşim türü aşağıdakilerden hangisinde sırasıyla doğru olarak verilmiştir?
A) İyonik - Apolar Kovalent - Polar Kovalent
B) İyonik - Polar Kovalent - Apolar Kovalent
C) Polar Kovalent - İyonik - İyonik
D) Polar Kovalet - İyonik - Polar Kovalent
E) Apolar Kovalent - Polar Kovalent - İyonik -
Aşağıdaki cümleleri okuyarak doğru olan yargıların başına (D), yanlış olana (Y) yazınız
[......] Elementler sembol, bileşikler ise formüllerle gösterirler.
[......] Rutherford, atomun yapısında büyük boşluklar olduğu fikrini ileri sürmüştür.
[......] Paschen ışıması, n=4,5,6... seviyelerinden n=3 seviyesine olan ışımaları ifade eder.
[......] Pauli’ nin Belirsizlik Kuramı’ na göre bir elektronun yeri ve hızı aynı anda tespit edilemez.
[......] Triatlar Kuramı olarak bilinen kural ilk kez Alexander John Newlans tarafından ortaya atılmıştır. -
Aşağıda verilen cümlelerde verilen boşlukları uygun kavramlarla doldurunuz
a. Modern periyodik tabloda elemetler, artan ……………..numaralarına göre yan yana sıralanmışlardır.
b. ………………… ‘ ya göre dört temel element; “Hava, Toprak, Su ve Ateş” tir.
c. Periyodik tabloda 3. Periyot 5A grubunda bulunan element, …………..sembolü ile gösterilir.
d. Periyodik tablonun 4 ve 5 nci periyotlarında …………’ er tane element bulunmaktadır.
e. 2A grubu elementleri olarak bilinen elementlerin özel adı …………………………….Metalleridir. -
Aşağıdakilerden hangisi periyodik sistemin oluşuman katkı sunmamıştır?
A) Mendelev B) Moseley C) Franklin
D) Meyer E) Döbereiner -
Mdern periyodik tablo ile ilgili aşağıdakilerden hangisi yanlıştır?
A) Yatay sıralara periyot denir.
B) Düşey sütunlara grup denir.
C) Eşit sayıda grup ve periyot vardır.
D) Elementler artan atom numaralarına göre sıralanmıştır.
E) Her element için sadece bir tane kutucuk ayrılmıştır. -
I. Bir atomun elektron sayısı kadar iyonlaşma enerjisi vardır.
II. Kolay kopan elektronlara değerlik elektronları denir.
III. Aynı grupta yukarıdan aşağıya doğru inildikçe iyonlaşma enerjisi azalır.
Yukarıda verilen ifadelerden hangisi veya hangileri doğrudur?A) I, II ve III B) I ve III C) I ve II
D) II ve III E) Yalnız I -
I. Elementlerin fiziksel ve kimyasal özelliklerinin değişimi atom yarıçapına bağlıdır.
II. Periyodik sistemde aynı grupta yukarıdan aşağıya doğru katma sayısı arttıkça atom yarıçapı artar.
III. Aynı periyotta soldan sağa doğru katman sayısı değişmez.
Yukarıda verilen ifadelerden hangisi veya hangileri doğrudur?A) I, II ve III B) I ve III C) I ve II
D) II ve III E) Yalnız I -
Aşağıdakilerden hangisi ametal değildir?
A) H B) C C) N D) O E) B
-
Aşağıdakilerden hangisi yarı metaller için doğru değildir?
A) Metallerle ametallerin arasında yer alırlar.
B) Parlak veya mat olabilirler.
C) Gaz halinde bulunurlar.
D) Hem pozitif hem de negatif yüklü iyon haline geçebilirler.
E) Hem metallerin hem de ametallerin özelliklerini taşırlar. -
I. Periyodik sistemde elementlerin büyük çoğunluğunu oluşturur.
II. Genellikle son katmanlarında 1, 2, 3 elektron bulundururlar.
III. Hidrojen ve bor hariç 1A, 2A 3A grupları, geçiş ve iç geçiş elementleri metaldir.
Metallerle ilgili yukarıda verilenlerden hangisi veya hangileri doğrudur?A) Yalnız I B) I ve II C) II ve III
D) I ve III E) I, II ve III -
I. Yatay satırlara periyot denir.
II. Düşey sütunlara grup denir.
III. 7 periyot ve 18 gruptan oluşur.
Modern periyodik tablo ile ilgili yukarıda verilenlerden hangisi veya hangileri doğrudur?A) Yalnız I B) I ve II C) II ve III
D) I ve III E) I, II ve III -
Kütle numaraları aynı, nötron ve atom numaraları farklı olan atomlara ................. atomlar denir.
Yukarıda verilen boşluğa hangisi getirilmelidir?A) izotop B) izoton C) izobar
D) izoelektronik E) izoprotonik -
Nötron sayıları aynı, proton sayıları faklı olan atomlara ................. atomlar denir.
Yukarıda verilen boşluğa hangisi getirilmelidir?A) izotop B) izoton C) izobar
D) izoelektronik E) izoprotonik
Doğru cevap B şıkkıdır. B şıkkında "H2" olarak verilen örnek, hidrojen molekülünü doğru bir şekilde temsil etmektedir. Diğer şıklar da doğru örnekler içermektedir.
doğru cevap C) Metalik Özellik'tir. Soy gazlar, periyodik tabloda en sağda bulunan elementlerdir. Soy gazlar tamamen dolu olan dış elektron kabuğuna sahip oldukları için metalik özellikleri bulunmaz. Diğer taraftan, periyot boyunca ilerledikçe metalik özellikler genellikle azalır
doğru cevap D şıkkı olacaktır. Çünkü Ca ve Cl atomları arasındaki bağ iyoniktir ve bileşiğin formülü CaCl2'dir. Bu soru, öğrencilerin kararlı iyonların Lewis yapılarını ve bağ türlerini anlama becerisini ölçmeyi amaçlamaktadır.
Bu sorunun cevabı C şıkkıdır, yani I, II ve III bağ türleri atomlar arası bağ türlerini temsil eder. İyonik bağlar, iyonlar arasında oluşan elektriksel çekim kuvvetine dayanır. Kovalent bağlar, atomlar arasında elektron paylaşımıyla oluşur. Metalik bağlar ise metal atomlarının denge durumunda serbestçe hareket eden elektronlar arasındaki çekime dayanır. Hidrojen bağları ise hidrojen atomunun elektronegatif bir atomla oluşturduğu zayıf bağlardır.
Doğru cevap D) Ne ve Mg'dir. Elif, Ne atomunun Lewis yapısını doğru bir şekilde yazmıştır, çünkü Ne atomunda 8 değerlik elektronu bulunur ve Lewis yapısında sekiz nokta ile temsil edilir. Ancak, Mg atomunun Lewis yapısını yanlış yazmıştır, çünkü Mg atomunda 2 değerlik elektronu bulunur ve Lewis yapısında iki nokta ile temsil edilir.
Doğru cevap A seçeneğidir (11). Soruda belirtilen element 2. periyot 2A grubunda bulunuyor, bu nedenle proton sayısı 2'dir. Nötron sayısı ise proton sayısından 3 fazla olduğu belirtiliyor, yani nötron sayısı 2 + 3 = 5'tir. Kütle numarası ise proton sayısıyla nötron sayısının toplamıdır, yani 2 + 5 = 7'dir. Doğru cevap 11 olmalıdır. Özür dilerim ve teşekkür ederim, hatamı düzelttiğiniz için.
Hayır, cevap anahtarı C) 3. Periyot 1A Grubu olmalıdır.- X^+ iyonu, elektron kaybetmiş bir iyon olduğu için 10Ne atomu ile aynı elektron sayısına sahiptir. - 10Ne atomu, 10 elektron içerir. Dolayısıyla, X atomunun da 10 elektron içermesi gerekir. - 3. periyotta yer alan 1A Grubu elementleri, 10 elektronlu atomlardır. - Bu nedenle, X atomunun periyodik sistemdeki yeri 3. Periyot 1A Grubu olmalıdır.
Doğru cevap D seçeneğidir. I - B eşleştirmesi, "Metallerin ısı ve elektrik iletim yeteneği" tanımına doğru karşılık gelmektedir. II - C eşleştirmesi, "Aynı elementin farklı atom sayılarına sahip izotopları" tanımına doğru karşılık gelmektedir. III - A eşleştirmesi, "Bir bileşiğin oluşumu sırasında veya sonrasında salınan enerji" tanımına doğru karşılık gelmektedir.
Doğru cevap A seçeneğidir, yani CO bileşiğinin adı yanlıştır. CO bileşiği karbon monoksit olarak adlandırılır, bu nedenle soruda verilen adı olan "Karbon dioksit" yanlıştır. Diğer seçeneklerdeki bileşiklerin adları doğrudur.
. Doğru cevap A seçeneğidir. Çözüm açıklamasında, 11X7Y9Z elementlerinin yaptıkları X3Y, Y2 ve Y2Z moleküllerinin molekül içi etkileşim türleri doğru olarak sıralanmıştır. İlk molekül X3Y, iyonik bağlar içerir çünkü X ve Y arasında elektron transferi gerçekleşir. İkinci molekül Y2, apolar kovalent bağlar içerir çünkü Y atomları arasında elektron paylaşımı gerçekleşir. Üçüncü molekül Y2Z, polar kovalent bağlar içerir çünkü Y ve Z arasında elektron paylaşımı gerçekleşir.
1. (D) Elementler sembol, bileşikler ise formüllerle gösterirler.
2. (Y) Rutherford, atomun yapısında büyük boşluklar olduğu fikrini ileri sürmüştür.
3. (Y) Paschen ışıması, n=4,5,6... seviyelerinden n=3 seviyesine olan ışımaları ifade eder.
4. (D) Pauli'nin Belirsizlik Kuramı'na göre bir elektronun yeri ve hızı aynı anda tespit edilemez.
5. (Y) Triatlar Kuramı olarak bilinen kural ilk kez Alexander John Newlans tarafından ortaya atılmıştır.
Açıklama:1. Doğru (D). Elementler sembolle gösterilirken, bileşikler formüllerle gösterilir. Bu temel kimya bilgisidir. 2. Yanlış (Y). Rutherford, atomun yapısında büyük boşluklar olduğunu değil, atomun çekirdeğinde yoğun bir pozitif yük olduğunu keşfetmiştir. 3. Yanlış (Y). Paschen serisi, hidrojen atomunun n=3 seviyesine olan ışımalarını ifade eder. 4. Doğru (D). Pauli'nin Belirsizlik İlkesi, bir elektronun hem konumunun hem de momentumunun tam olarak belirlenemeyeceğini ifade eder. 5. Yanlış (Y). "Triatlar Kuramı" olarak bahsedilen bir kural bulunmamaktadır.
a. atom numaralarına b. Antik dönemlere c. Bor d. 18'er e. Alkali
Açıklama:a. Modern periyodik tabloda elementler, artan atom numaralarına göre yan yana sıralanmıştır. Atom numarası, bir elementin çekirdeğinde bulunan proton sayısını temsil eder. b. Antik dönemlere göre dört temel element; "Hava, Toprak, Su ve Ateş"tir. Bu antik felsefi kavram, modern kimyada kullanılan elementlerin temel yapı taşlarını ifade etmektedir. c. Periyodik tabloda 3. Periyot 5A grubunda bulunan element, Bor sembolü (B) ile gösterilir. Periyodik tablo, elementleri benzer özelliklere sahip gruplara ve sıralara göre düzenler. d. Periyodik tablonun 4 ve 5. periyotlarında 18'er tane element bulunmaktadır. Her periyot, artan atom numaralarına göre yeni bir elektron kabuğu eklenerek oluşur. e. 2A grubu elementleri olarak bilinen elementlerin özel adı "Alkali Metalleridir." Alkali metaller, periyodik tablonun 2A grubunda bulunurlar ve genellikle reaktif ve metalik özelliklere sahiptirler.
Cevap anahtarı: C) Franklin Periyodik sistemin oluşumunda katkısı olmayan kişi C) Franklin'dir. Franklin, periyodik sistemin oluşumuna katkıda bulunmamıştır. Diğer seçenekler ise periyodik sistemin oluşumunda önemli roller oynayan bilim insanlarıdır. Mendelev, periyodik tabloyu ilk kez düzenleyen ve elementlerin periyodik tekrarlanan özelliklerini keşfeden bilim insanıdır. Moseley, elementlerin atom numaralarıyla sıralanmasına dayanan modern periyodik tabloyu geliştiren bilim insanıdır. Meyer ve Döbereiner ise elementlerin kimyasal özelliklerindeki periyodik tekrarlanma hakkında çalışmalar yapmışlardır.
Doğru cevap C) Eşit sayıda grup ve periyot vardır. İfade A doğrudur. Yatay sıralamalara periyot adı verilir. Periyotlar, benzer özelliklere sahip elementlerin yan yana olduğu sıralamalardır. İfade B doğrudur. Düşey sütunlara grup adı verilir. Gruplar, benzer kimyasal özelliklere sahip elementlerin aynı dikey sütunda yer aldığı bölümlerdir. İfade C yanlıştır. Eşit sayıda grup ve periyot bulunmaz. Grup sayısı periyot sayısından daha fazladır. İfade D doğrudur. Elementler periyodik tabloda artan atom numaralarına göre sıralanmıştır. İfade E doğrudur. Her element için periyodik tabloda ayrı bir kutucuk bulunur.
Doğru cevap anahtarı A) I, II ve III'dür. I. ifade doğrudur. Bir atomun elektron sayısı kadar iyonlaşma enerjisi vardır. İyonlaşma enerjisi, bir atomun bir elektronunu kaybetmek için gereken enerji miktarını ifade eder. II. ifade doğrudur. Kolay kopan elektronlara değerlik elektronları denir. Değerlik elektronları, bir atomun en dış elektron kabuğundaki elektronları ifade eder. III. ifade doğrudur. Aynı grupta yukarıdan aşağıya doğru inildikçe iyonlaşma enerjisi genellikle azalır. Elektron kabukları daha fazla enerji seviyesine yayıldıkça atomun tutma kuvveti zayıflar ve iyonlaşma enerjisi azalır.
Doğru cevap A) I, II ve III olmalıdır. İfade I doğrudur. Elementlerin fiziksel ve kimyasal özellikleri atom yarıçapına bağlı olarak değişir. Atom yarıçapı, elektron dağılımı ve atomun genel büyüklüğü hakkında önemli bir bilgidir. İfade II doğrudur. Periyodik sistemde, aynı grupta yukarıdan aşağıya doğru ilerledikçe katman sayısı ve elektron sayısı artar, bu da atom yarıçapının genellikle artmasına yol açar. İfade III doğrudur. Aynı periyotta soldan sağa doğru katman sayısı değişmez. Periyodik tabloda aynı periyotta bulunan elementlerin elektron dizilimi aynı katmanlarda gerçekleşir.
Cevap anahtarı: E) B Verilen seçenekler arasında ametal olanlar H (Hidrojen), C (Karbon), N (Azot) ve O (Oksijen)'dur. Bu seçenekler ametaldir. Ancak, B (Bor) seçeneği bir metaloiddir, yani metal ve ametal özelliklerine sahip bir elementtir, bu nedenle ametal değildir.
Cevap Anahtarı: C) Gaz halinde bulunurlar. 1. İfade A doğrudur. Yarı metaller, metallerle ametallerin arasında yer alan elementlerdir. Hem metal hem de ametallerin özelliklerini kısmen sergilerler. 2. İfade B doğrudur. Yarı metaller, parlak veya mat olabilen farklı görünümlere sahip olabilirler. Örneğin, silisyum mat bir görünüme sahipken, arsenik parlak bir görünüme sahiptir. 3. İfade C yanlıştır. Yarı metaller, genellikle katı veya bazen sıvı formda bulunurlar. Gaz halinde bulunma özelliği genellikle ametaller için geçerlidir. 4. İfade D doğrudur. Yarı metaller, hem pozitif hem de negatif yüklü iyonlara dönüşebilirler. Bu özellik, yarı metallerin elektron alışverişine katıldığını ve iyonlaşma yeteneklerini gösterir. 5. İfade E doğrudur. Yarı metaller, hem metallerin hem de ametallerin bazı özelliklerini taşırlar. Örneğin, elektriksel iletkenlik özelliği gibi bazı metal özelliklerini sergilerken, kırılganlık gibi ametallerin özelliklerini de gösterebilirler.
Cevap anahtarı: E) I, II ve III I. ifade doğrudur. Periyodik sistemde elementlerin büyük çoğunluğu metallerdir. Metaller periyodik tablonun sol tarafında bulunurlar. II. ifade doğrudur. Genellikle metallerin son katmanlarında 1, 2 veya 3 elektron bulunur. Bu elektronlar kolaylıkla kaybedilebilir ve pozitif iyonlar oluşabilir. III. ifade doğrudur. Hidrojen ve bor dışında, 1A, 2A ve 3A grupları, geçiş metalleri ve iç geçiş metalleri gibi metaldir. Bu gruplar periyodik tablonun sol tarafında yer alır.
Cevap anahtarı: E) I, II ve III I. ifade doğrudur. Yatay satırlara periyot denir. Periyotlar, periyodik tabloda elementlerin benzer özelliklere sahip olan gruplarda sıralandığı yatay sıralardır. II. ifade doğrudur. Düşey sütunlara grup denir. Gruplar, periyodik tabloda elementlerin aynı dikey sütunda bulunduğu ve benzer kimyasal özelliklere sahip olduğu sütunlardır. III. ifade doğrudur. Modern periyodik tablo 7 periyot ve 18 grup içerir. Periyodik tablo, elementlerin benzer özelliklere sahip gruplara ve sıralara göre düzenlendiği bir yapıyı temsil eder.
Doğru cevap anahtarı C) izobar olacaktır. Verilen boşluğa C) izobar getirilmelidir. İzobarlar, kütle numaraları (nükleon sayısı) farklı ancak nötron ve atom numaraları aynı olan atomlardır. Bu durumda, izobarlar farklı elementlere ait olacaktır.
Doğru cevap B) izoton olmalıdır. İzotoplar, aynı elementin farklı atomlarıdır ve nötron sayıları aynı olmasına rağmen proton sayıları farklıdır. İzotonlar, nötron sayıları farklı olmasına rağmen proton sayıları aynı olan atomlardır. Farklı elementlerin izotonları birbirinden farklı özelliklere sahiptir. İzobarlar, toplam nükleon sayıları aynı olmasına rağmen nötron sayıları farklı olan atomlardır. İzoelektronik, aynı elektron dizilimine sahip olan farklı atomlardır. Elektron sayısı aynı olduğu için benzer kimyasal özelliklere sahiptirler. İzoprotonik terimi kullanılmayan bir terimdir.
Yorum Bırak
2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test Detayları
2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test 16 kere indirildi. Bu sınav Zor derecede zorluktadır. Sınav zorluk derecesi sınavı oluşturan soruların istatistikleri alınarak oluşturulmuştur. Toplamda 22 sorudan oluşmaktadır. Sınav soruları aşağıda verilen kazanımları ölçecek şekilde hazırlanmıştır. 16 Aralık 2022 tarihinde eklenmiştir. Bu sınavı şimdiye kadar 1 kullanıcı beğenmiş. Bu sınavı çözerek başarınızı artırmak için 2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test Testini Çöz tıklayın. 2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test yazılı sınavına henüz hiç yorum yapılmamış. İlk yorum yapan siz olun.2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test sınavında hangi soru türleri kullanılmıştır?
Bu sınavda verilen soru türleri kullanılmıştır.- Test
- Doğru-Yanlış
- Boşluk Doldurma
- Test
2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test Hangi Kazanımları Kapsıyor?
Bu sınav ve tema ve kazanımlarını kapsamaktadır.- ATOM VE PERİYODİK SİSTEM
- Atom Modelleri
- Atomun Yapısı
- Periyodik Sistem
Ayrıca 2022-2023 9.sınıf kimya dersi 1.dönem 2.yazılı soruları; tamamı test ve cevap anahtarlı olarak yeni müfredat uygun hazırlanmıştır
Kimyasal türlerin doğru tanımlanması ve örneklerinin bilinmesi hedeflenir.
Periyodik tablodaki elementlerin özelliklerini ve periyotlar arası geçişlerdeki trendleri anlamaktır.
İyonik bağ oluşturan elementlerin bileşik formülasyonunu doğru bir şekilde belirleyebilmeleri hedeflenir.
Bağ türlerini tanıma ve farklı bağ türlerini ayırt etme becerisini ölçmeyi amaçlamaktadır.
Atomların Lewis yapısını doğru bir şekilde çizme becerisini ve değerlik elektronlarının yerleşimini anlamaktır. Lewis yapısı, atomun değerlik elektronlarını ve bu elektronların kimyasal bağlarda nasıl paylaşıldığını gösteren bir gösterimdir.
Periyodik tablodaki elementlerin kütle numaralarını ve proton-nötron ilişkisini anlama becerisini ölçmeyi amaçlamaktadır.
Periyodik cetveldeki elementlerin yerlerini ve gruplarını anlamaları beklenir.
Kimyasal türleri ve tanımlarını doğru bir şekilde eşleştirebilmelerini ölçmeyi amaçlamaktadır.
Formüllerini ve adlarını eşleştirebilme yeteneklerini geliştirmeleri beklenir.
Moleküller arasındaki bağ türlerini anlamalarını ve elementler arasındaki etkileşimleri doğru bir şekilde tanımlamalarını amaçlamaktadır.
Atom ve Elektron Yapısı konusunda bilgi.
Periyodik tabloda elementlerin atom numarasına, sembollerine ve gruplara göre sıralandığını ve periyotlarda belirli sayıda element bulunduğunu öğrenilir.
Periyodik sistemin oluşumuna katkıda bulunan bilim insanlarının isimlerini ve katkılarını öğrenilir.
Modern periyodik tablonun yapısal özellikleri ve terimleri hakkında bilgi.
İyonlaşma enerjisinin tanımını bilmek, değerlik elektronlarının ne olduğunu anlamak ve periyodik tablodaki trendlere dair bilgi sahibi olmak.
Atom yarıçapı, periyodik tablonun yapısal özellikleri ve periyodik tablodaki trendler hakkında bilgi.
Ametal olan elementleri tanımak ve metaloid elementleri ayırt etmek.
Yarı metallerin tanımı, özellikleri ve genel özelliklerini anlama.
Metallerin periyodik tabloda genellikle büyük bir çoğunluğu oluşturduğunu, son katmanlarında belirli sayıda elektron taşıdıklarını ve 1A, 2A ve 3A gruplarının metal elementlerden oluştuğunu öğrenilir.
Periyotların ve grupların periyodik tablodaki konumlarını anlamak, elementlerin benzer özelliklere sahip gruplarda sıralandığını ve periyodik tablonun belirli bir düzeni olduğunu öğrenilir.
İzobarların kütle numaraları farklı olmasına rağmen nötron ve atom numaralarının aynı olduğunu anlamak.
İzotonların tanımı ve özellikleri hakkında bilgi.
etiketlerini kapsamaktadır.Hangi kategoriye ait?
2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test sınavı 9.Sınıf kategorisinin Kimya alt kategorisinin, 1 dönemine ait.2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test Testi İstatistikleri
Bu sınav 69 kere çözüldü. Sınava kayıtlı tüm sorulara toplamda 352 kere doğru, 404 kere yanlış cevap verilmiş.2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test Sınavını hangi formatta indirebilirim?
2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test sınavını .pdf veya .docx olarak ücretsiz indirebilirsiniz. Bunun yanında sistem üzerinden doğrudan yazdırabilirsiniz. Veya öğretmen olarak giriş yaptıysanız 2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test sınavını sayfanıza kaydedebilirsiniz.2022-2023 9.Sınıf Kimya 1.Dönem 2.Yazılı - Test sınav sorularının cevap anahtarlarını nasıl görebilirim?
Sınavın cevap anahtarını görebilmek için yukarıda verilen linke tıklamanız yeterli. Her sorunun cevabı sorunun altında gösterilecektir. Veya Sınavı .docx olarak indirdiğinizde office word programıyla açtığınızda en son sayfada soruların cevap anahtarına ulaşabilirsiniz.Kendi Sınavını Oluştur
Değerli öğretmenlerimiz, isterseniz sistemimizde kayıtlı binlerce sorudan 9.Sınıf Kimya dersi için sınav-yazılı hazırlama robotu ile ücretsiz olarak beş dakika içerisinde istediğiniz soru sayısında, soru tipinde ve zorluk derecesinde sınav oluşturabilirsiniz. Yazılı robotu için Sınav Robotu tıklayın.
Sınav hakkında telif veya dönüt vermek için lütfen bizimle iletişime geçin.
Paylaşın
Sınavı İndir
.docx vey .pdf9.Sınıf Kimya Dersi Benzer Sınavları
9.Sınıf İçin Eklenen Son Sınavlar
-
9.Sınıf Astronomi ve Uzay Bilimleri 2.Dönem 2.Yazılı - Klasik
Lise Astronomi ve Uzay Bilimleri 2.Dönem Sonu Yazılı - Açık Uçlu Sorular
9.Sınıf Astronomi ve Uzay Bilimleri Sene Sonu Yazılı - Klasik
9.Sınıf Astronomi ve Uzay Bilimleri 2.Dönem 2.Yazılıya Hazırlık Test 1
Lise Astronomi ve Uzay Bilimleri 2.Dönem 2.Yazılıya Hazırlık Test 2